La unidad quimica de concentración es esencial en la química y la bioquímica, ya que nos permite expresar de manera cuantitativa la cantidad de una sustancia disuelta en una solución o mezcla. Estas unidades nos permiten comprender y controlar la cantidad de soluto presente en una solución, lo que es fundamental para la preparación de soluciones químicas con la concentración adecuada para una amplia variedad de aplicaciones, desde la investigación en laboratorios hasta la fabricación de productos industriales.
En este contexto, existen diversas unidades de concentración, como molaridad, molalidad, porcentaje en peso y volumen, entre otras, cada una con su propia aplicación y significado. En este párrafo introductorio, exploraremos la importancia y la diversidad de esta unidad quimicas de concentración en el mundo de la química y la ciencia.
¿Que son las unidades de concentración?
Las unidades de concentración son medidas cuantitativas que se utilizan en química para expresar la cantidad relativa de una sustancia disuelta en una solución o mezcla.
Estas unidad quimica de concentracion proporcionan información sobre la proporción del soluto (la sustancia que se disuelve) con respecto al solvente (el medio en el que se disuelve) o al total de la solución. Existen varias unidades de concentración comunes, entre las cuales se incluyen:
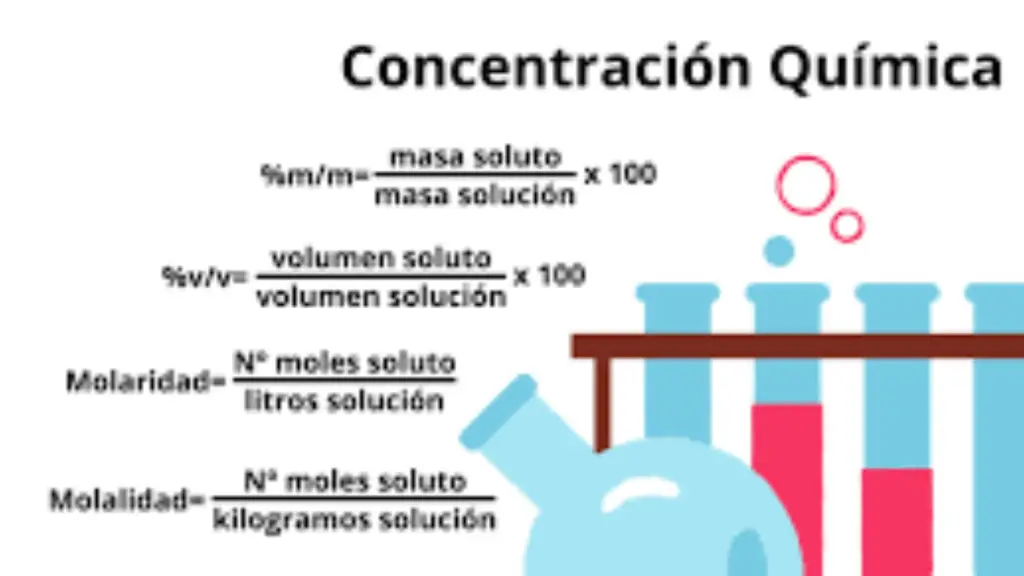
- Molaridad (M): Expresa la cantidad de moles de soluto por litro de solución. Es especialmente útil en reacciones químicas donde se requiere conocer la concentración de reactivos o productos.
- Molalidad (m): Indica la cantidad de moles de soluto por kilogramo de solvente. Se utiliza en situaciones en las que la temperatura puede variar y la molaridad no es constante.
- Porcentaje en masa (% en masa): Representa la masa del soluto en relación con la masa total de la solución, multiplicada por 100. Se expresa como porcentaje (%).
- Porcentaje en volumen (% en volumen): Indica el volumen del soluto en relación con el volumen total de la solución, multiplicado por 100. Es común en la preparación de mezclas en la industria, como las soluciones de alcohol y agua.
- Fracción molar (X): Describe la fracción de moles del soluto en relación con el número total de moles en la solución. Se utiliza principalmente en termodinámica y mezclas de gases.
- Normalidad (N): Es similar a la molaridad, pero se basa en equivalentes de soluto en lugar de moles. Se utiliza en reacciones que involucran transferencia de electrones, como las reacciones redox.
- Partes por millón (ppm) y partes por billón (ppb): Expresan la concentración en términos de una cantidad de soluto en relación con un millón o mil millones de partes del total, respectivamente. Se usan en situaciones donde las cantidades de soluto son extremadamente pequeñas.
La elección de la unidad quimica de concentración depende de la aplicación específica y las propiedades del sistema químico que se esté estudiando o manipulando. Cada unidad proporciona información valiosa sobre la concentración de una sustancia en una solución y su relevancia en un contexto particular.
Unidades de concentracion porcentual
Las unidades de concentración porcentual expresan la cantidad de soluto en una solución como un porcentaje de la masa total o el volumen total de la solución. Algunas de las unidades de concentración porcentual más comunes incluyen:
- Porcentaje en masa (% en masa o % p/p): Esta unidad expresa la masa del soluto en relación con la masa total de la solución y se calcula mediante la siguiente fórmula:
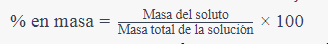
- Porcentaje en volumen (% en volumen o % v/v): Indica el volumen del soluto en relación con el volumen total de la solución y se calcula de la siguiente manera:

- Porcentaje en peso-volumen (% p/v): Se utiliza para expresar la concentración de un soluto sólido en un solvente líquido. Indica la masa del soluto en relación con el volumen total de la solución y se calcula como:

- Porcentaje en volumen-volumen (% v/v): Se emplea para soluciones líquidas y representa el volumen del soluto en relación con el volumen total de la solución. La fórmula es:

Estas unidades de concentración porcentual son ampliamente utilizadas en laboratorios, industrias y aplicaciones cotidianas para expresar la concentración de solutos en diversas soluciones, como soluciones químicas, productos farmacéuticos, bebidas, alimentos, productos de limpieza, entre otros. La elección de la unidad depende de la naturaleza de la solución y el contexto de la medición.
