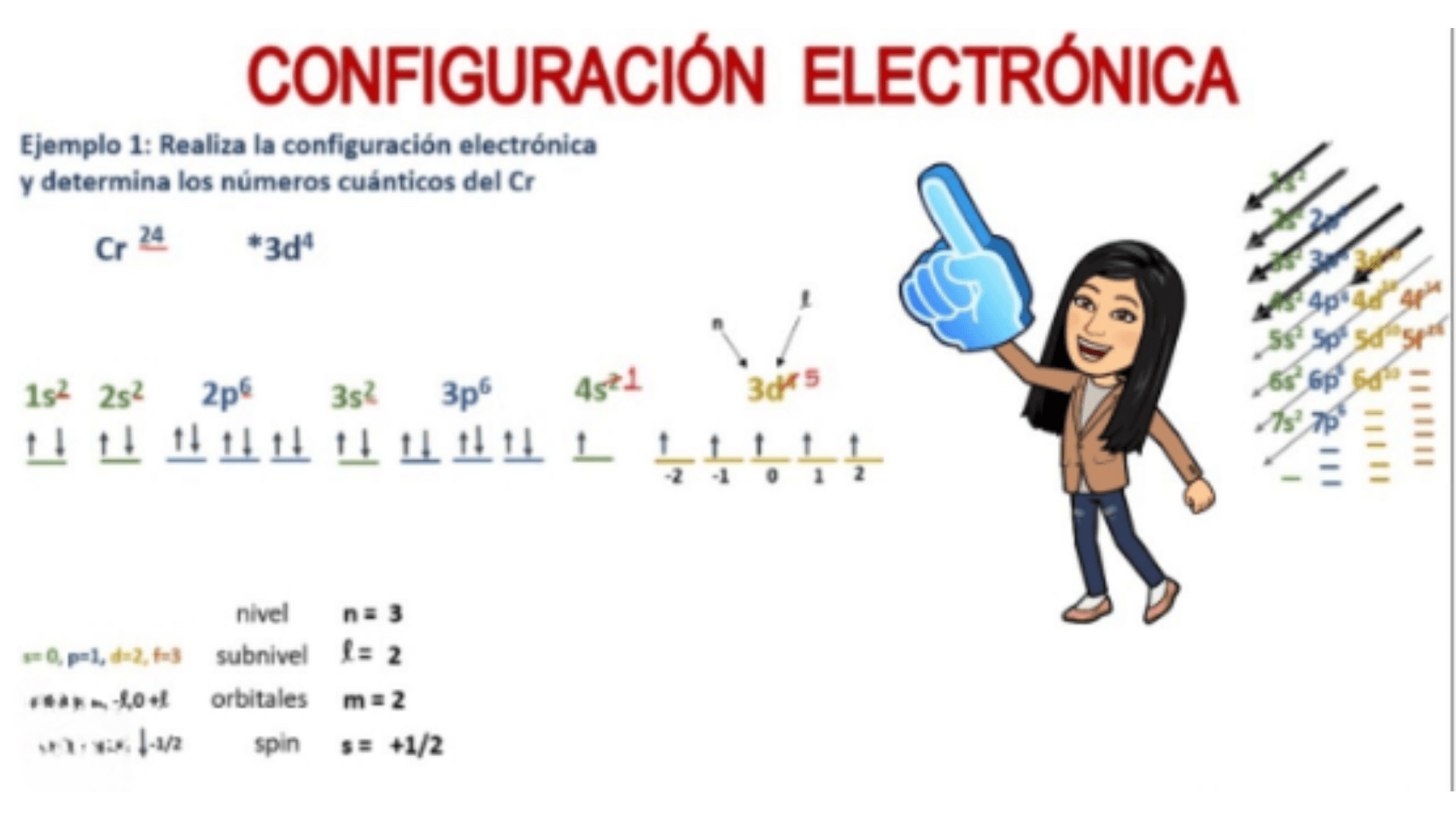
La configuración electrónica de un elemento se refiere a la distribución de electrones en diferentes niveles de energía (capas electrónicas) de un átomo. Esta distribución se describe utilizando números cuánticos y notaciones especiales.
Los números cuánticos son números enteros que describen las propiedades de los electrones en un átomo.
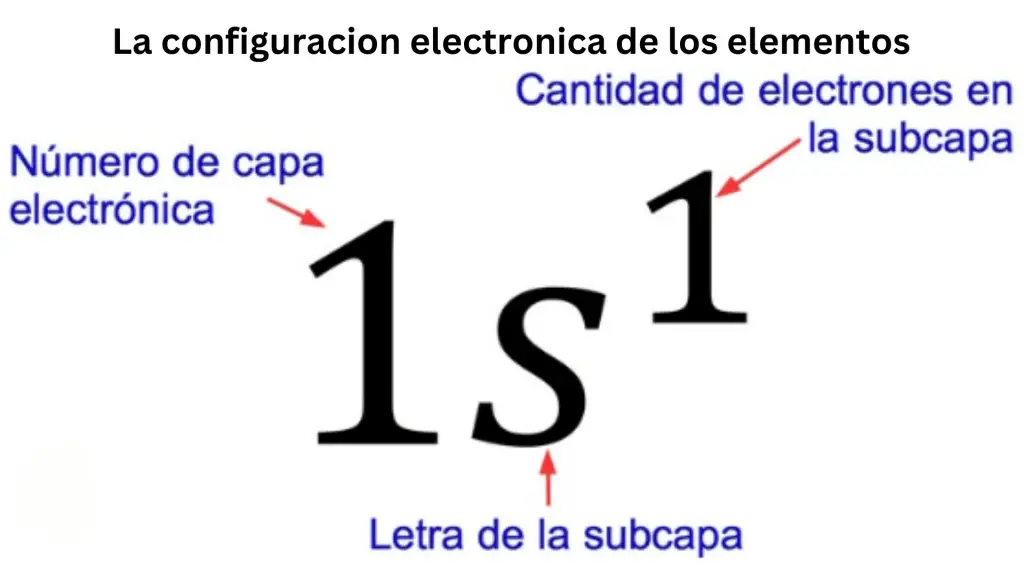
La notación general para la configuración electrónica de un átomo se expresa de la siguiente manera:
Número atómico (Z): representa el número de protones en el núcleo de un átomo y por tanto también el número de electrones en un átomo neutro.
Configuración electrónica en cada capa: la notación se realiza enumerando las capas de electrones (niveles de energía) con números enteros (n=1, n=2, n=3, etc.) e indicando el número de electrones en cada nivel de energía.
Por ejemplo, para el hidrógeno (H) con número atómico 1, su configuración electrónica es simplemente 1s¹, lo que significa que tiene un electrón de primera capa (n=1) en el orbital 1s.
Para el oxígeno (O) con número atómico 8, su configuración electrónica es 1s² 2s² 2p⁴, lo que indica que tiene dos electrones en la primera capa (1s²) y seis electrones en la segunda capa (2s² 2p⁴).
Es importante recordar que existen ciertas reglas para llenar orbitales de energía según el principio de Pauli, el principio de Aufbau y la regla de Hund.
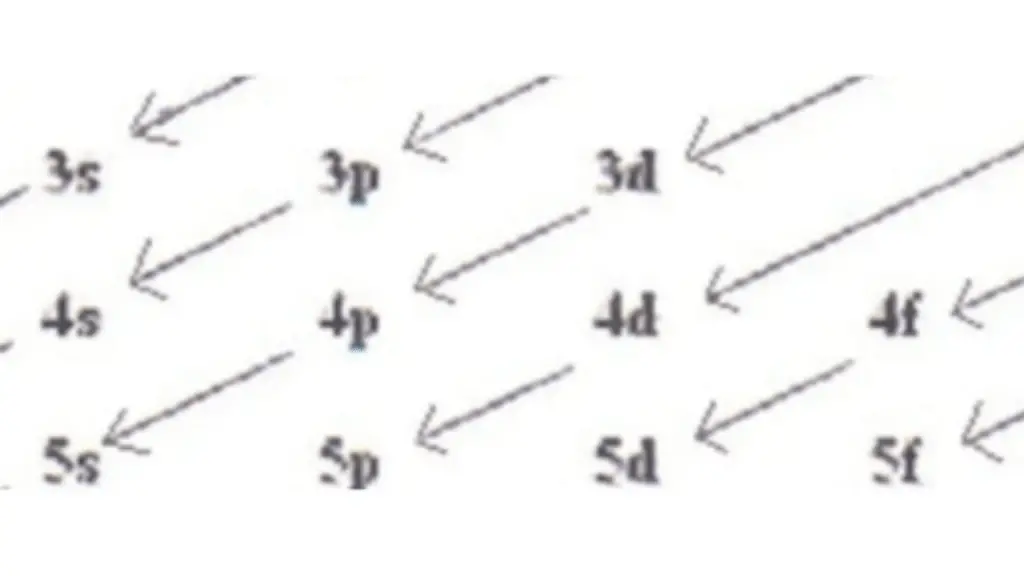
Estas reglas determinan la secuencia en la que los electrones llenan los orbitales y aseguran que se llenen de manera eficiente.
Por tanto, la configuración electrónica es una descripción de cómo se distribuyen los electrones en los diferentes niveles de energía de un átomo y está representada por números cuánticos y notaciones especiales.